1. VARIÁVEIS DE ESTADO
Todo gás é constituído de partículas (moléculas, átomos ou íons) que estão em contínuo movimento desordenado, por isso ocupa sempre o volume total do recipiente que o contém. A pressão que o gás exerce sobre uma superfície é o efeito causado pelos choques das partículas constituintes sobre essa superfície. Com o aumento da temperatura, a velocidade média das partículas constituintes do gás aumenta; a pressão aumenta se o recipiente que contém o gás conserva o mesmo volume. Sejam P (Pa), V (m3) e T (K), respectivamente, a pressão, o volume e a temperatura absoluta. As variáveis P, V e T especificam o estado de uma dada massa gasosa; por isso são denominadas variáveis de estado.
2. TRANSFORMAÇÕES DOS GASES
Uma dada massa sofre uma transformação gasosa quando passa a um novo estado, isto é, quando ocorrem variações nas grandezas P, V e T. Há transformações mais simples, onde uma das grandezas é fixa, modificando-se apenas as outras duas. Transformação isotérmica é aquela na qual a temperatura do gás é mantida constante.
Transformação isobárica é aquela na qual a pressão do gás é mantida constante.
Transformação isométrica ou isocórica é aquela na qual o volume do gás é mantido constante.
3. GASES PERFEITOS OU IDEAIS
São aqueles que (só existem teoricamente) obedecem à risca a equação geral dos gases perfeitos.
Os gases reais apresentam comportamentos que se aproximam dos ideais quanto mais baixa for a pressão e mais alta sua temperatura.

Observações: Quando nos referimos a uma dada massa gasosa, nas transformações, isto significa que a equação geral dos gases perfeitos só se aplica para massa constante do gás, no estado inicial e final. Ao se referir a condições normais de temperatura e pressão, abreviadamente CNTP, a temperatura considerada é 273K e a pressão de 1 atm (105 Pa). As variáveis de estado são medidas:
T - temperatura medida no termômetro. V - volume do gás é o volume do recipiente. P - pressão medida no manômetro.
Lei de Boyle-Mariotte:
Na transformação isotérmica de uma dada massa gasosa, a pressão é inversamente proporcional ao volume.


O diagrama anterior P x V denomina-se diagrama de Clapeyron e a isoterma é o conjunto de todos os pontos de mesma temperatura.
Lei de Charles (1ª Lei de Gay-Lussac):
Na transformação isobárica de uma dada massa gasosa, o volume é diretamente proporcional à temperatura absoluta.


Lei de Charles (2ª Lei de Gay-Lussac):
Na transformação isométrica (isocórica) de uma dada massa gasosa, a pressão é diretamente proporcional à temperatura absoluta.


fonte : http://www.fisica.net/einsteinjr/7/comportamento_termico_dos_gases.html



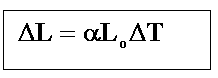
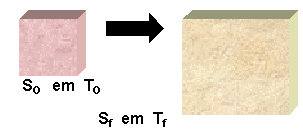

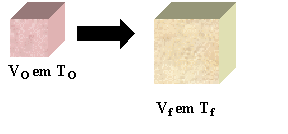
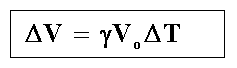


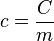
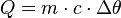
 (o corpo se aquece).
(o corpo se aquece). (o corpo se esfria).
(o corpo se esfria).
 ) a partir da
) a partir da 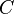 ) e da
) e da  ).
).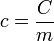
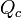 ), da massa desse corpo, e da variação térmica (
), da massa desse corpo, e da variação térmica ( ) que ele sofre (temperatura final - temperatura inicial).
) que ele sofre (temperatura final - temperatura inicial).